一、实验目的
1. 掌握容量瓶的规格和使用方法;
2. 掌握配置一定物质的量浓度的溶液的方法,熟悉实验的误差分析。
二、实验用品
1. 仪器和材料:
天平、100mL容量瓶、量筒、烧杯、玻璃棒、胶头滴管、称量纸、药匙
2. 药品:
碳酸钠固体、蒸馏水
三、实验内容
1. 容量瓶的使用
(1)构造:容量瓶由瓶体和瓶塞两部分组成,使用前须检验容量瓶是否漏水。
(2)特点:容量瓶上标有温度、容积和刻度线;
(3)规格:容量瓶体积固定,常见的有:50 mL、100 mL、250 mL、500 mL、1000 mL等。
(4)使用:在容量瓶所标记的温度下,当溶液的凹液面正好与刻度线相切时,容量瓶中溶液的体积正好等于容量瓶的规格。
2. 配置一定物质的量浓度的溶液
(1)计算:根据配制要求计算出所需固体溶质Na2CO3:
0.100 mol/L-1 × 0.100 L × 105.99g/mol-1 = 1.06 g。
(2)称量:用天平称量固体溶质Na2CO3 1.06 g。
(3)溶解:将称量的溶质放入烧杯中再加入适量的蒸馏水,用玻璃棒搅拌使之溶解,并放置冷却至室温。
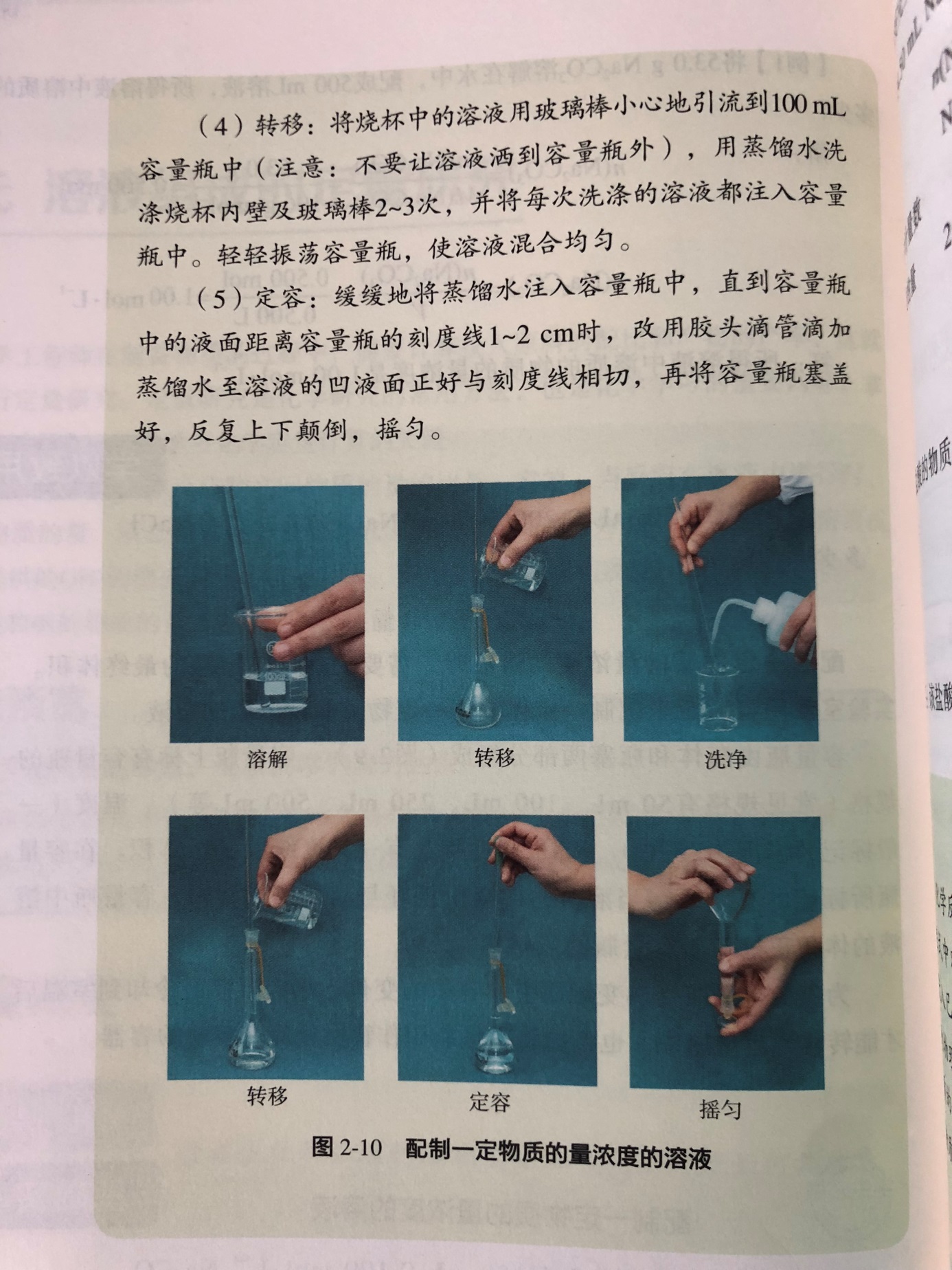
(4)转移:将溶解冷却至室温的溶液,沿玻璃棒注入准备好的100 mL容量瓶中,并用适量蒸馏水洗涤烧杯内壁和玻璃棒2-3次,并将洗涤液转移至容量瓶中。轻轻震荡容量瓶,使溶液混合均匀。
注意:玻璃棒应放置在容量瓶刻度线以下,倾倒时不要让溶液洒在容量瓶外,也不要让溶液在刻度线上沿瓶壁流下。
(5)定容:缓缓地将蒸馏水注入容量瓶中,直到容量瓶中的液面距离容量瓶的刻度线1-2cm时,改用胶头滴管逐滴加入蒸馏水直到凹液面最低点与刻度线水平相切。
(6)摇匀:盖好容量瓶塞,反复上下颠倒,摇匀。
(7)装瓶贴签:将配好的溶液装入干净试剂瓶中,贴上标签,注明名称、浓度、配制日期。
四、注意事项
1. 使用前要检查是否漏水(检漏):加水-盖塞-倒立观察-若不漏-正立,旋转塞子180°-再倒立观察-不漏则可使用;
2. 配制一定体积的溶液时,容量瓶的规格必须与要配制的溶液的体积相同;
3. 使用时手握容量瓶的瓶颈刻度线以上部位;
4. 溶解或稀释的操作不能在容量瓶中进行;
5. 溶解时放热的必须冷却至室温后才能移液;
6. 定容后,经反复颠倒,摇匀后会出现容量瓶中的液面低于容量瓶刻度线的情况,这时不能再向容量瓶中加入蒸馏水;
7. 如果加水定容时超过了刻度线,不能将超出部分再吸走,必须重新配制;
8. 容量瓶只能用来配制溶液,不能存放溶液或进行化学反应。
五、误差分析
1. 容量瓶使用前未干燥,容量瓶中含有少量水
2. 称量时间过长
3. 称量前小烧杯内有水
4. 未冷却到室温就注入容量瓶定容
5. 转移液体时少量流出
6. 转移后未洗涤烧杯和玻璃棒
7. 洗涤液未转入容量瓶
8. 往容量瓶中加水时有少量加到瓶外
9. 定容时仰视刻度线
10. 定容时俯视刻度线
11. 定容时水多用滴管吸出
12. 定容摇匀时液面下降,再加水至刻线
13. 定容时液面低于刻度线
14. 定容摇匀后,有少量溶液流出
附教材内容:苏教版 高中必修一 第35-37页 【基础实验-学生必做实验】